- La Valtria nelle notizie -
Particolarità delle GMP nella progettazione di strutture per la cannabis terapeutica
1. Introduzione
Le Buone Pratiche di Fabbricazione (GMP) non sono standard e linee guida, come possono essere le ISO, ma sono direttive europee (2003/94/CE), che sono state recepite nella legislazione spagnola con il Real Decreto 2183/2004.
Nell’introduzione e nella conclusione, che sono obbligatorie.
Il loro aspetto di “direttiva” lascia un certo livello di interpretazione, che si riduce di giorno in giorno grazie ai risultati delle ispezioni, alle deviazioni ufficiali e al supporto della letteratura. Negli Stati Uniti, le cGMP (c=current) ci aiutano a ridurre questo margine di interpretazione.
Per “legge” siamo obbligati a garantire la produzione di prodotti “sicuri, di qualità ed efficienti”.
Le varie normative che riguardano le GMP forniscono una guida per ridurre questo margine di interpretazione. Questo ci permette di implementare le migliori pratiche nella progettazione e nel funzionamento delle strutture. L’obiettivo rimane lo stesso: garantire un risultato sicuro, efficiente, affidabile e stabile nel tempo.
Va ricordato che uno standard non è obbligatorio finché non viene emesso un decreto legge. Va notato che le GMP menzionano l’ICH e l’ISO 14644. Questi standard satellitari o obbligatori sono stati sviluppati per definire con maggiore precisione i processi e le attività “sensibili”.
L’elevato numero di processi di produzione dei prodotti farmaceutici ha portato alla creazione di questi standard, per cui, ad eccezione di casi particolari, i percorsi finiscono per essere abbastanza chiari.
Ma non offrono nemmeno risposte definitive e concrete per ogni caso, cosa che sarebbe impossibile con l’infinito numero di prodotti, ma lasciano al produttore il compito di giustificare le soluzioni implementate per rispettare le GMP.
Questo porta a uno degli strumenti più discussi e con più letteratura, “l’analisi dei rischi” (generalmente su un processo), che guida in ogni caso sulle azioni preventive (progettazione, procedure), organizzative e operative da implementare.
In questo articolo affrontiamo alcune particolarità dell’applicazione delle normative sulla cannabis terapeutica, oltre alla grande importanza dell’implementazione degli standard GACP (Good Agricultural and Collection Practices).
2. Cannabis medica
La cannabis è un caso particolare nell’ambito delle pratiche di produzione dei farmaci standard per i seguenti motivi:
- Sebbene esistano molti farmaci o API e integratori a base vegetale, questi raggiungono il consumatore finale/paziente sotto forma di estratti.
- Nessun altro farmaco, come la cannabis, è disponibile nella sua forma floreale originale, a parte i formati convenzionali (tralasciamo le formule erboristiche, che sono gradualmente scomparse dalla farmacopea e che non rientrano nella definizione di farmaci con effetto terapeutico).
- La cannabis è un’API molto potente, con molteplici combinazioni di componenti (cannabinoidi, terpeni) e molteplici applicazioni terapeutiche, alcune delle quali con effetti collaterali o psicotropi (con relative implicazioni sulla sicurezza).
- Le caratteristiche principali della cannabis come API sono date dalla genetica, ma durante la crescita della pianta può cambiare notevolmente la sua potenza (concentrazione).
- La cannabis ha aperto le porte a un nuovo profilo professionale al di fuori del settore della produzione farmaceutica, il che ha portato a discrepanze nell’applicazione delle norme GMP in questo processo.
3. Implementazione delle norme GMP
Vediamo alcune particolarità dell’applicazione di questi standard GMP nella produzione di cannabis, sulla base della nostra esperienza e delle nostre analisi dei rischi di prodotto e di processo per la cannabis.
Fiore essiccato di Cannabis "uso diretto" come prodotto medicinale.
Secondo la tabella 1 dell’applicazione delle linee guida GMP alla produzione di principi attivi di origine vegetale, ci collocheremmo in terza fila:
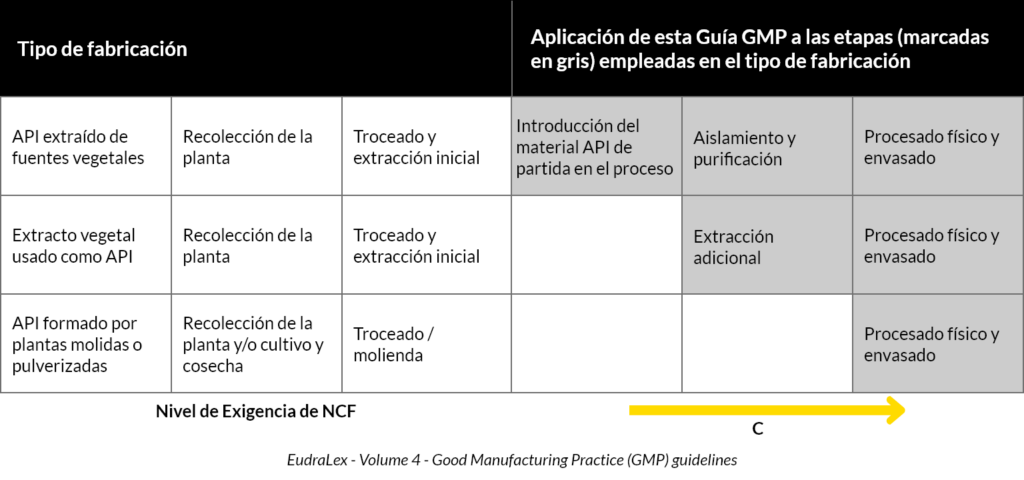
Seguendo le indicazioni della tabella, gli standard GMP inizieranno a essere applicati al momento della lavorazione fisica e del confezionamento, compresi l’essiccazione e la rasatura (ultime fasi di lavorazione prima della dispensazione ai pazienti).
Poiché gli standard GMP si applicano solo alle fasi finali di lavorazione, l’applicazione degli standard GACP durante le fasi di coltivazione è di particolare importanza per i seguenti aspetti:
- I diversi principi attivi vengono creati in un ambiente non controllato (secondo i criteri farmaceutici) per più di 10 settimane, si tratta di un caso atipico. Se facciamo un parallelo con la formulazione di un API, le GMP si applicano nel momento in cui compare la molecola attiva. In questo caso, invece, la molecola attiva appare e si forma molto prima di entrare nei requisiti delle GMP.
- Le condizioni ambientali (temperatura, umidità e luce), così come i processi e le strategie di coltivazione (densità, irrigazione, fertilizzanti, …) influenzano notevolmente la composizione dei diversi API e la resa del raccolto.
- Qualsiasi parametro fuori controllo può invalidare completamente il prodotto. Sapendo che le GMP non sono obbligatorie, l’applicazione delle GACP diventa ancora più importante.
- La valutazione dei fornitori, la formazione del personale, le condizioni delle strutture richiedono procedure molto rigorose, anche se non si tratta di GMP.
È fondamentale controllare i diversi parametri che compongono la fase di coltivazione per garantire la qualità, la stabilità e la resa del raccolto.
Allo stesso tempo, tenere sotto controllo i parametri sopra citati comporta un aumento dei costi di investimento e di gestione, quindi è necessario trovare un equilibrio.
Fiore essiccato di Cannabis "uso diretto" come medicinale
Quando si tratta di definire la classificazione dell’ambiente controllato per la lavorazione della cannabis, torniamo alle GMP e non abbiamo una risposta chiara. Nell’allegato 7 si dice semplicemente di attuare particolari misure per evitare la contaminazione incrociata.
Dal Capitolo 1 del nuovo Allegato 1 e i suoi “principi e linee guida, come la strategia di controllo della contaminazione, la progettazione dell’impianto, la classificazione della camera bianca, la qualificazione, la convalida, il monitoraggio e l’abbigliamento del personale, possono essere utilizzati per supportare la produzione di altri prodotti che non sono destinati a essere sterili, come alcuni liquidi, creme, unguenti e intermedi biologici con un basso carico microbico, ma in cui il controllo e la riduzione della contaminazione microbica sono considerati importanti”.
Non ci resta che scegliere di passare alla ISO 8, come precauzione minima per rispondere alle caratteristiche di questo prodotto. Ma perché non un’altra classificazione?
Diamo un’occhiata ad alcune particolarità:
- Si tratta di una produzione “mono-prodotto”, ma a causa di alcuni lunghi tempi di lavorazione (essiccazione, polimerizzazione) diversi lotti possono coincidere nello spazio di produzione.
- A differenza di altri prodotti farmaceutici, il rischio di contaminazione incrociata non deriva dalle miscele di principi attivi, anche se vengono lavorate genetiche diverse.
- Il rischio maggiore è quello biologico (funghi, batteri…), proveniente dal prodotto stesso o da agenti esterni. Questa contaminazione biologica può essere evidente e rilevabile nelle prime fasi GMP e nei primi controlli di qualità del lotto, oppure rimanere latente e svilupparsi nei primi giorni della fase di essiccazione, dove le condizioni ambientali sono ancora adatte alla proliferazione di funghi e batteri.
- Secondo la nostra analisi, il rischio maggiore di contaminazione incrociata si avrebbe nelle sale di lavorazione e asciugatura a umido. Per questi locali consigliamo di progettare pressioni di contenimento e procedure rigorose per quanto riguarda i DPI e le azioni correttive in caso di rilevamento di contaminazione.
- È importante notare che durante il processo il prodotto è esposto per molto tempo (anche giorni) all’ambiente del locale che funge da contenitore. Pertanto, le procedure di pulizia e disinfezione dei locali devono essere esaustive. Si torna quindi all’allegato 1, con l’obbligo di sviluppare un’accurata CCS, “Strategia di Controllo della Contaminazione”, adatta a questa peculiarità, ovvero che per la maggior parte del tempo il locale, l’ambiente, con i suoi operatori, viene assimilato al contenitore, fino alla fase di confezionamento.
Definizione del lotto
Nelle GMP si fa sempre riferimento al lotto di produzione, cioè a una quantità fissa di prodotto ottenuto nelle stesse condizioni e con lo stesso processo per garantire l’uniformità. Questo implica una grande complessità nel caso della cannabis terapeutica. Una volta che l’applicazione delle GACP garantisce la massima uniformità, nei limiti delle possibilità delle strutture di coltivazione disponibili, il processo GMP assicura il mantenimento di questa uniformità:
- I processi sono lenti (la lavorazione di un lotto può durare da uno a due turni di lavoro) ed esposti a un ambiente a cui è sensibile. Questo ambiente deve essere adeguato e controllato per garantire che il primo e l’ultimo prodotto lavorato abbiano le stesse caratteristiche.
- Nel caso dell’essiccazione, si tratta di un grande volume di prodotto che è un materiale “vivo”, che si evolve nel corso di diversi giorni. Gli impianti devono essere progettati in modo ottimale e debitamente convalidati (mappatura della temperatura e dell’umidità, ricette di essiccazione, procedure di riempimento, ecc.)
- Molti processi richiedono l’intervento umano. Pensa a diverse fasi, ad esempio la rasatura manuale o il tempo e le condizioni di indurimento, in cui le decisioni sono soggettive.
- Infine, la dimensione di ogni lotto, dopo il lungo processo di oltre 100 giorni dall’ottenimento delle talee al prodotto finale, può variare notevolmente. La riconciliazione tra il numero di piante, gli scarti, i rifiuti e il prodotto finale ottenuto è molto complessa e critica nel caso di una sostanza stupefacente.
Fiore per estratti di Cannabis terapeutica
A questo punto, ci troveremmo nella prima e seconda riga della tabella 1 (applicazione delle linee guida GMP).
Secondo la nostra esperienza, nel caso di un prodotto in cui viene effettuata una sola estrazione, questa deve essere effettuata in un ambiente GMP. D’altra parte, se c’è un’estrazione più una distillazione o una purificazione, l’estrazione può essere effettuata in un ambiente NON GMP, a patto che le fasi successive siano necessariamente eseguite in un ambiente GMP.
Più il prodotto da ottenere è purificato, maggiore è la variabilità che può avere il materiale di partenza (fiore), anche se avremo un impatto importante sulla resa (costi) del nostro processo. Questa variabilità nelle caratteristiche dei fiori ci permetterebbe di avere un’infrastruttura di coltivazione meno specializzata, ma non ci esime dalla stretta osservanza degli standard GACP, poiché una fonte vegetale fuori dai parametri non ci permette di rispettare gli standard del processo GMP.
Per le estrazioni a spettro completo (prima estrazione) in cui si valuta la presenza di altri cannabinoidi o terpeni, il punto di partenza è costituito da genetiche molto specifiche che vengono addirittura associate alla descrizione che accompagna il prodotto finale. La qualità del fiore di partenza è fondamentale (corrisponderebbe alla funzione di un reattore per API chimici). Per questa qualità di “fiore GMP per l’estrazione”, è necessario che il responsabile del farmaco sia coinvolto nella definizione del processo produttivo.
4. Conclusioni
Ci rendiamo conto che fare luce su come applicare le norme GMP sulla cannabis terapeutica nella produzione di questo particolare medicinale richiede una conoscenza dettagliata del prodotto e del processo. Dobbiamo cercare parte delle risposte nel nuovo Allegato 1 e costringerci a sviluppare un CCS con una base scientifica di analisi dei rischi.
Questo approccio GMP al processo di produzione della cannabis terapeutica (certificato dall’AEMPS), oltre a garantire la qualità e la stabilità dei prodotti, è il passo fondamentale e obbligatorio per considerare la cannabis come una medicina e la terrà lontana dalla percezione negativa della società.
5. Bibliografia
- Buone pratiche di fabbricazione dei medicinali: Direttiva 2003/94/CE della Commissione (Direttiva (UE) 2017/1572 della Commissione per i medicinali per uso umano – in particolare allegato 7, allegato 1).
- ICHQ9: Gestione del rischio di qualità_2005
- ICHQ7A: Ingredienti farmaceutici attivi GMP
- ICH Q10: SISTEMA DI QUALITÀ FARMACEUTICA
- Pharmacopoea Helvetica 11.3 Ed-fr_2019 : Fiore di cannabis, CH211-S-263
- Monografia analitica Cannabis Flos – WTO / Farmalyse BV V7, 28.11.2014
- Bundesinstitut für Arzneimittel und Medizinprodukte Bekanntmachung zum Deutschen Arzneibuch 2018* Vom 9. April 2018
- GUIDA PIC/S ALLE BUONE PRASSI DI FABBRICAZIONE DEI MEDICINALI
Eudald Bogatell
Ingegnere di progetto presso VALTRIA